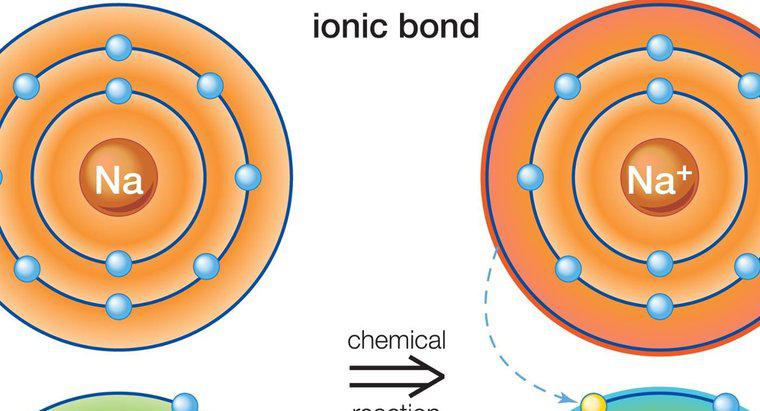
Denumirea compușilor ionici necesită identificarea corectă a speciilor cationice și anionice prezente. În anumite cazuri, încărcarea ionului este importantă pentru denumirea precisă.
Principiile de denumire chimică standard identifică mai întâi cationul în denumire și al doilea anion. În compușii ionici, cationul este în mod obișnuit un metal, iar prima parte a numelui compusului este pur și simplu metalul. Dacă cationul poate exista natural în stări multiple încărcate, sarcina metalului, cunoscută și sub numele de valență, trebuie identificată în denumirea compusului cu cifre romane. De exemplu, fierul poate exista în starea pozitivă cu două sau pozitive, cu trei sarcini. Acestea ar fi numite fier (II) și fier (III), respectiv.
Pasul final în denumirea unui compus ionic este identificarea corectă a anionului prezent. Anionii pot fi un singur ion, cum ar fi bromura, sau molecule complexe care sunt alcătuite din mai mulți atomi, cum ar fi sulfatul. Pentru acești anioni complexi există parametri suplimentari de denumire. Elementele care sunt capabile să formeze mai multe oxianii, cum ar fi azotul și sulful, au fie un sfârșit, fie un sfârșit, în funcție de numărul de molecule de oxigen prezente. Un exemplu de compus ionic numit în mod corespunzător este sulfatul de fier (II) pentru formula ionică Fe (SO4).