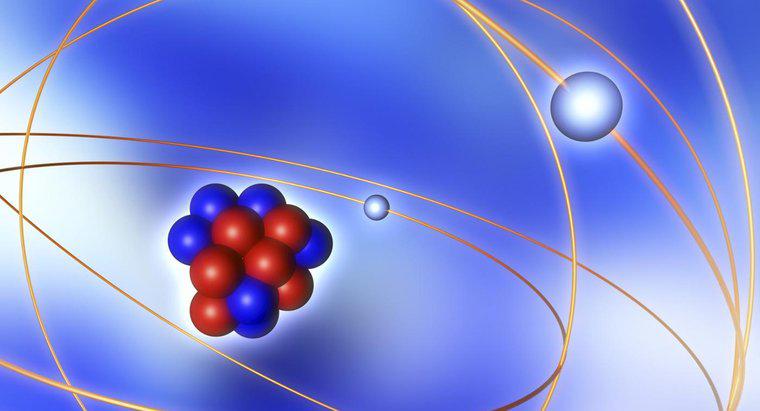
Nucleul unui atom conține neutroni și protoni. Protonii sunt încărcați pozitiv, în timp ce neutronii sunt neutri. Electronii, în timp ce fac parte din atom, nu fac parte din nucleu.
Atomii sunt neutri din punct de vedere electric, ceea ce înseamnă că au o cantitate egală de încărcare negativă și pozitivă. Încărcarea netă a nucleului unui atom este pozitivă din cauza protonilor pozitivi. Pentru a contracara acest lucru, electronii încărcați negativ orbitează nucleul.
Un atom neutru are același număr de protoni ca și electronii. Spre deosebire de protoni, numărul de neutroni din nucleu poate varia. Un atom care conține cantitatea corectă de protoni și electroni, dar cu un număr diferit de neutroni în nucleu, se numește izotop.
Majoritatea masei unui atom este localizată în nucleu. Electronii sunt mult mai ușori decât protonii și neutronii.
Chiar dacă un nucleu conține cea mai mare parte a masei unui atom, este foarte mic în comparație cu dimensiunea totală a atomului. Acest lucru se datorează faptului că protonii și neutronii sunt ținute strâns împreună de forța nucleară. Fără această forță nucleară, protonii pozitivi s-ar opune reciproc și nucleul nu ar exista. Dacă forța nucleară este prea slabă, nucleul se descompune, ducând la emisii radioactive.