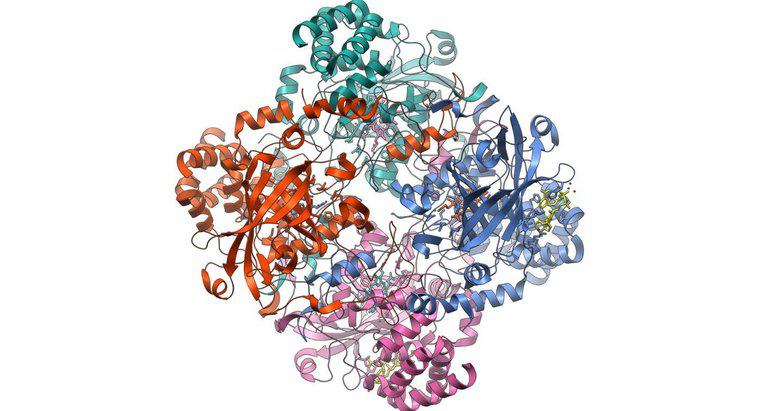
Hemoglobina leagă oxigenul prin rugină la nivelul atomic. Moleculele hemoglobinei din celulele roșii din sânge sunt ceea ce Departamentul de Științe al Departamentului de Energie al SUA numește o "metaloproteină". Aceasta este o proteină care încorporează în structura ei un metal, fier în acest caz. Fiecare moleculă de hemoglobină poartă patru atomi legați de fier care lucrează în mod cooperativ pentru a transporta oxigen din plămâni, de unde este abundent, în alte părți ale corpului.
Potrivit site-ului Web al Centrului Național pentru Biotehnologii, atomii de fier purtați de hemoglobină reacționează la prezența oxigenului în mod similar cu cel al fierului, prin legarea cu acesta într-un proces numit oxidare. Compusul rezultat, oxid de fier, se numește rugina atunci când se găsește în afara corpului. În interiorul celulelor roșii din sânge, aceste molecule oxidate de hemoglobină se mențin pe încărcătura lor cu oxigen până când ajung la o parte a corpului care nu are suficient oxigen, unde este eliberat.
Același articol observă că cele patru subunități ale moleculei de hemoglobină lucrează împreună pentru a lega oxigenul foarte eficient în medii bogate în oxigen, dar efectul slăbește în mediile în care oxigenul este slab. Această reacție inegală face hemoglobina dornică să se lege cu oxigen în plămâni și la fel de dornică să se despartă de ea în prezența unei celule înfundate de oxigen, după care ciclul începe de la început.