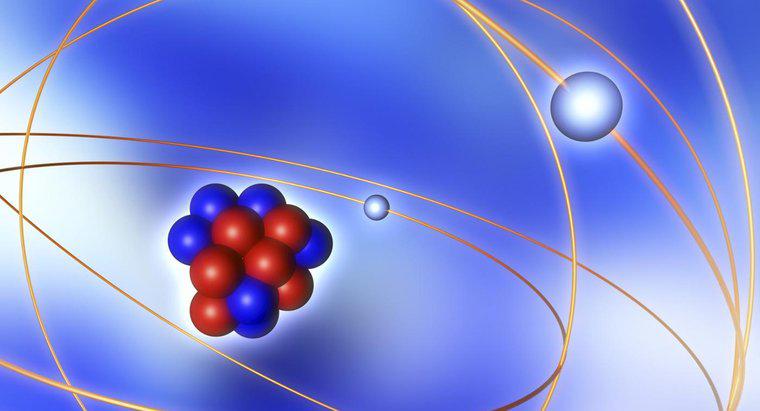
Nucleul unui atom este înconjurat de un nor de electroni care este menținut pe loc de o forță electromagnetică. Nucleul reprezintă mai mult din masa totală a atomului decât cloudul, deși conturile cloud pentru un volum mai mare de atom.
Un atom are trei blocuri: protoni, neutroni și electroni. Nucleul localizat central este alcătuit din protonii încărcați pozitiv și neutronii neutri. Aceste elemente sunt legate între ele de o forță nucleară. Numărul de protoni din nucleu determină ce element aparține atomului, denumit în mod obișnuit numărul atomic. Norul de electroni din jur este compus în întregime din electroni încărcați negativ. În ciuda nucleului și a norului înconjurător, cea mai mare parte a unui atom este spațiu gol.
Modelul nor nu a fost primul concept. Mai multe modele au fost luate în considerare înainte ca norul să fie acceptat în anii 1920. Modelele anterioare au inclus modelele Billiard Ball și Plum Pudding. Modelul Bohr a fost adoptat în secolul al XX-lea. În acest model, atomul este similar cu un sistem solar.
Un electron are o încărcătură de 1.0671 x 10 ^ -19 coulomb. O proprietate importantă a electronilor este spinul. Spinarea pe un electron este o rată specifică de 1/2 ori o unitate de rotație, care poate fi atribuită de către persoana care efectuează măsurarea.