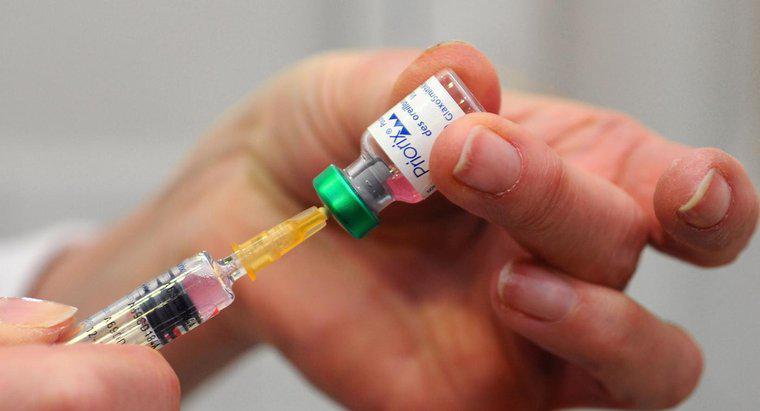
O aplicație practică a legii lui Boyle atrage fluidul într-o seringă. Tragerea înapoi a pistonului mărește volumul interior al seringii și îi reduce presiunea. Fluidul din exteriorul seringii este aspirat în cilindru până când presiunea interioară și exterioară sunt echilibrate.
Legea lui Boyle precizează că volumul și presiunea unui gaz sau lichid rămân constante, cu condiția ca temperatura substanței să rămână aceeași. Această lege, care a fost declarată pentru prima dată de Robert Boyle în secolul al XVII-lea, este extrem de importantă în aplicațiile de inginerie, cum ar fi proiectarea motorului. Formula sa este V1 /V2 = P2 /P1 (la temperatura constanta), unde V1 este volumul initial, V2 este volumul modificat, P1 este presiunea de pornire si P2 este presiunea modificata.Legea cea mai apropiată legii lui Boyle este legea lui Charles sau "legea volumelor", care este lucrarea omului de știință francez Jacques Charles. Descrie relația dintre volum și temperatură. Atât legea lui Boyle, cât și legea lui Charles sunt teorii ale gazului care descriu comportamentul unui gaz ipotetic "ideal". În practică, totuși, ambele se aplică și lichidelor. Legea lui Boyle este numită uneori Legea lui Mariotte, o referire la cercetătorul francez care a descoperit aceleași principii la 14 ani după publicarea lui Boyle. Această convenție de numire este populară în Franța și în alte națiuni europene.