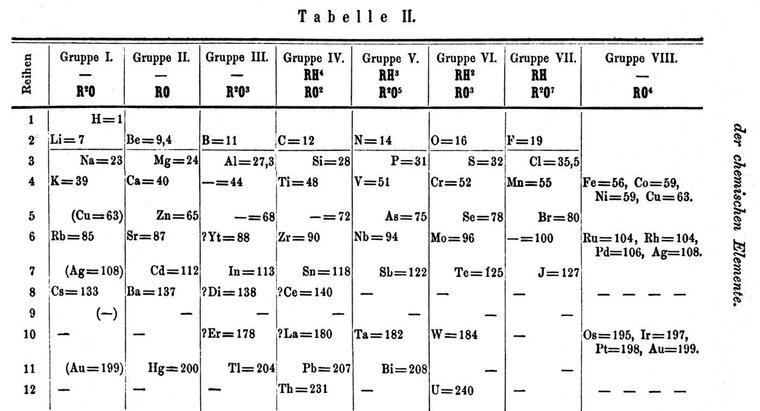
Chimistul rus, cunoscut ca tatăl mesei periodice, a văzut că unele elemente au apărut în locul greșit când au fost aranjate de greutățile lor atomice. De exemplu, el a văzut că un element ne-metal reactiv va fi urmat de un metal ușor de reacție și apoi va fi urmat de un metal ușor mai puțin reactiv. Mendeleev a ajuns la concluzia că, urmând care erau greutățile atomice asumate atunci, elementele au apărut în locuri unde proprietățile lor nu se potriveau cu cele ale vecinilor lor.
De ce Mendeleev nu aranjat elementele prin numerele lor atomice când a creat masa periodică?

Când Dmitri Mendeleev a creat tabelul periodic al elementelor, el a decis să nu le aranjeze prin numerele lor atomice, pe baza ipotezei lor corecte, conform căreia acele numere nu erau exacte. Când a început pentru prima dată să aranjeze 60 de elemente cunoscute în anii 1860, știa că în cele din urmă vor fi descoperite noi elemente, că există acum peste 100 de elemente cunoscute și că greutățile atomice ale elementelor cunoscute la acel moment fuseseră calculate incorect.