Deși fiecare atom este compus din particule de dimensiuni diferite, majoritatea spațiului sau volumului fiecărui atom constă în norul de electroni. Cu toate acestea, printre cele trei molecule prezente, neutronii sunt cele mai mari și nucleul atomului reprezintă 99,9% din masa totală.
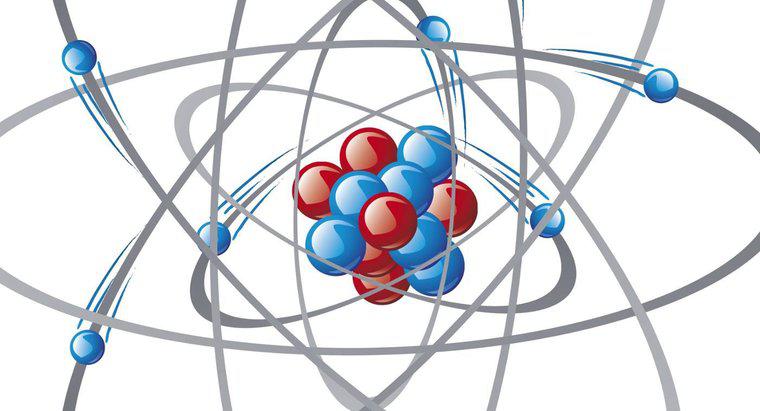
Structura de bază a oricărui atom include un nucleu format din protoni și neutroni și o serie de electroni mici care orbitează în jurul acestuia într-un spațiu numit nor de electroni. Singura excepție de la această structură este atomul de hidrogen, care nu conține neutroni.
Atomii, ca particulele pe care le formează, conțin mai mult spațiu gol decât masa, deoarece sarcina pozitivă a protonilor și încărcarea negativă a electronilor se repetă. Acest lucru creează ceea ce oamenii de știință numesc un "nor de electroni" care înconjoară nucleul fiecărui atom. În ceea ce privește volumul, norul de electroni constituie majoritatea "spațiului" fiecărui atom. O ilustrație obișnuită a acestui spațiu indică faptul că, dacă nucleul unui atom avea dimensiunea unei marmură, atunci marginea exterioară a norului de electroni ar fi mai mult de 100 de metri sau un câmp de fotbal, departe de el.
Totuși, în ciuda faptului că majoritatea spațiului fiecărui atom conține electronii, cea mai mare parte a lui, 99,9%, se află în nucleu. Masa nucleului atomului este împărțită aproape uniform între protoni și neutroni, deși neutronii sunt ușor mai mari. Masa electronilor, prin contrast, este egală cu 1/1836 a unui proton.