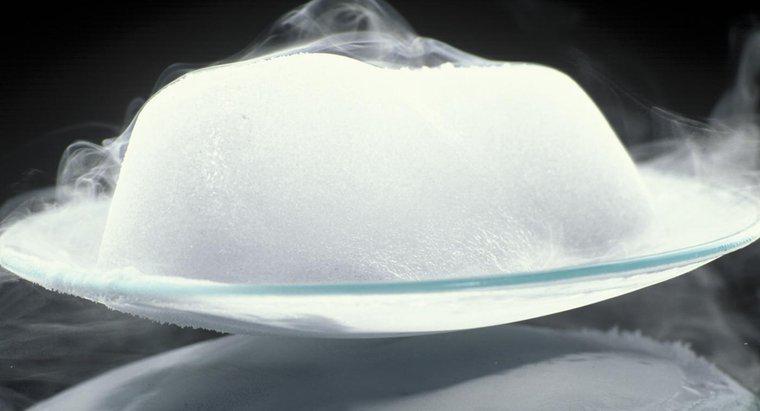
Sublimarea este schimbarea fazei de la un solid la un gaz. Este important de observat că faza lichidă nu este prezentă în sublimare.
Sublimarea are loc la temperaturi sub punctul triple al unei substanțe. Punctul triplu este o clipă în care toate cele trei faze ale materiei există în echilibru. Punctele triple sunt reprezentate pe diagramele de fază. În sublimare, substanța solidă este încălzită până la punctul în care aceasta se transformă în gaz fără a deveni mai întâi lichid.
Sublimarea este utilizată pentru purificarea substanțelor în procesele chimice. De obicei, practica începe prin plasarea unui solid într-un vas și apoi prin încălzirea acestuia în vid. Presiunea și căldura volatilizează solidul, transformând compusul într-un gaz. Impuritățile rămân solide în vas.
Sublimarea se aplică funcțiilor vopsirii și înghețării. În coloranți, cerneala este vaporizată de un încălzitor și apoi răcită pe hârtie sau țesătură. Ca rezultat, transferul de culoare este foarte definit și mai ușor de controlat, făcând posibilă o moarte mai complexă.
În congelatoare, o combinație de temperaturi sub zero și aer uscat, arid, împiedică formarea înghețului pe interior. Acest lucru este gestionat de un termostat intern și un ventilator. Cristalele de iod și dioxidul de carbon sunt exemple obișnuite de sublimare, deoarece sublimează la temperatura camerei.