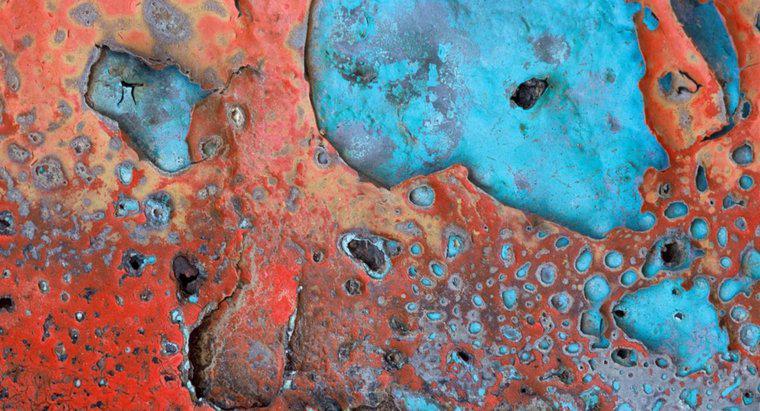Multe metale se oxidează și corodează, dar rugina sau oxidul de fier sunt specifice metalelor feroase, cum ar fi oțelul. Rugul se formează atunci când oxigenul se leagă cu un atom de fier pentru a forma o moleculă de oxid de fier. Această moleculă este considerabil mai mare decât moleculele de fier înconjurător, astfel încât aceasta devine rapid dislocată și se îndepărtează de pe suprafață. Acest lucru expune metale proaspete care pot, de asemenea, rugină.
Oxidarea fierului este o reacție care necesită trei componente: un electrolit, un anod și un catod. Un anod este un atom care dă un electron în timpul procesului, un catod este un alt atom care preia electronul și un electrolit este mediul prin care electronul poate călători. Fierul este foarte conductiv și poate acționa ca anod propriu, precum și catod. Electrolitul este adesea acid carbonic.
Acidul carbonic se formează atunci când o picătură de apă, de obicei ploaie, cade prin aer și preia o cantitate de dioxid de carbon. Acest dioxid de carbon se combină cu molecula de apă pentru a forma un compus oarecum acid, care degradează rapid orice anod potențial întâlnit. Pe o suprafață de fier, acidul carbonic permite fluxul de electroni de la unii atomi de fier, acționând ca anozi, la alți atomi de fier care acționează ca catozi. Procesul se mănâncă rapid prin suprafețe metalice și le lasă rotunjite și roșii sau maro.